A produção de insulina do paciente com diabetes tipo 1 restaurada com nova terapia de transplante de celular
28 de agosto de 2025
4 Min Read
Novo transplante de células para diabetes tipo 1 Necessidade de imunossupressores
Os cientistas trataram o diabetes tipo 1 de uma pessoa com células produtoras de insulina geneticamente modificadas que evitavam ataques do sistema imunológico. Esta é a primeira terapia para a condição que não requer drogas imunossupressoras
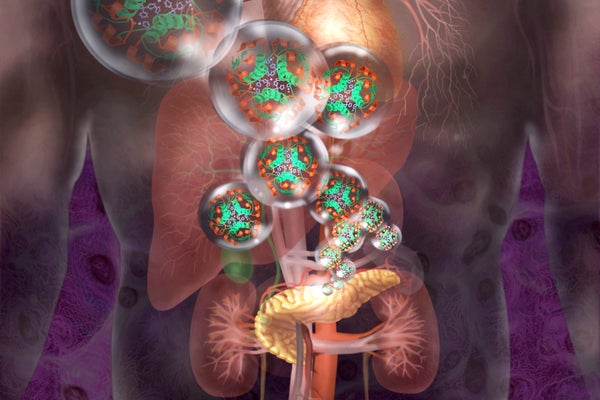
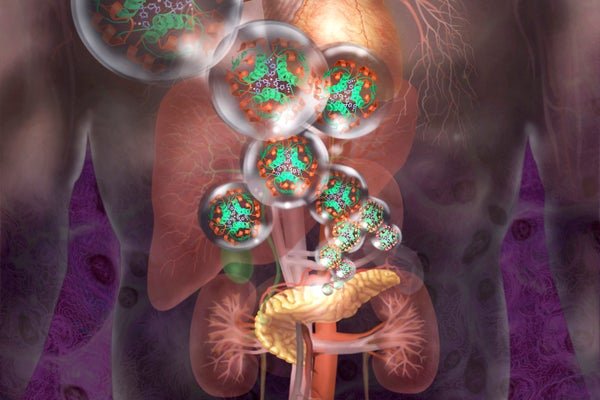
As células produtoras de insulina podem ser geneticamente modificadas para ocultar do sistema imunológico.
Jim Dowdalls/fonte de ciências
Pessoas com diabetes tipo 1 devem depender constantemente de injeções ou bombas de insulina, geralmente para o resto da vida após o diagnóstico. A doença auto -imune destrói as células que produzem o hormônio, que é crucial para manter o açúcar no sangue sob controle. Mas agora a pesquisa sugere que uma nova terapia poderia finalmente permitir que pessoas com diabetes tipo 1 façam insulina por conta própria.
Um homem de 42 anos que viveu a maior parte de sua vida com o diabetes tipo 1 se tornou o primeiro humano a receber um transplante de células geneticamente modificadas de produção de insulina que podem passar pelos ataques equivocados do sistema imunológico. Isso marca o primeiro transplante de células pancreáticas em um humano para evitar a necessidade de medicamentos imunossupressores – e pode até levar a uma cura futura para a doença, dizem os pesquisadores.
“Este é o momento mais emocionante da minha carreira científica”, diz o biólogo celular por Ola Carlsson, da Universidade de Uppsala, na Suécia, que ajudou a desenvolver o procedimento. O novo tratamento, ele diz, “abre a possibilidade futura de tratar não apenas o diabetes, mas outras doenças autoimunes”.
Sobre apoiar o jornalismo científico
Se você está gostando deste artigo, considere apoiar nosso jornalismo premiado por assinando. Ao comprar uma assinatura, você está ajudando a garantir o futuro das histórias impactantes sobre as descobertas e idéias que moldam nosso mundo hoje.
Os cientistas injetaram quase 80 milhões de células ajustadas geneticamente no músculo antebraço do participante e, 12 semanas depois, as células ainda estavam vivas e produzindo insulina. O destinatário exigiu injeções adicionais de insulina – mas as células injetadas não mostraram sinais de rejeição, o que os pesquisadores dizem ser um grande passo adiante. Os resultados foram relatados neste mês no New England Journal of Medicine.
Cerca de dois milhões de pessoas nos EUA vivem com diabetes tipo 1, o que normalmente requer um regime intensivo de injeções de insulina e monitoramento de açúcar no sangue. Se o açúcar no sangue correr, as pessoas enfrentam riscos graves, incluindo ataques cardíacos, danos nos nervos, problemas de visão, doença renal e muito mais.
Durante décadas, os cientistas lutaram para desenvolver terapias que podem reabastecer com sucesso as células beta-as células de produção de insulina especializadas que são encontradas no pâncreas. As células beta funcionais recém -adicionadas são geralmente destruídas rapidamente porque um sistema imunológico diabético tipo 1 as sinaliza como invasores. Algumas tentativas anteriores transplantaram com sucesso ilhotas de doador – clusters de células pancreáticas que incluíam células beta – mas elas sempre acabaram desencadeando uma resposta imune agressiva. E essa resposta exige que os destinatários tomem medicamentos imunossupressores ao longo da vida, que vêm com efeitos colaterais graves, como maiores riscos de infecções e câncer. Por exemplo, em uma conferência em junho, a Vertex Pharmaceuticals, com sede em Boston, anunciou que 10 dos 12 participantes que foram tratados com uma infusão baseada em células-tronco durante um ensaio clínico não exigiam mais injeções de insulina um ano após a terapia. Mas eles podem continuar a precisar imunossupressores.
No novo estudo, Carlsson e sua equipe procuraram maneiras de evitar a resposta imune. Primeiro, eles quebraram as ilhotas pancreáticas de um doador falecido em células únicas. Usando a técnica comum de edição de genes CRISPR, os pesquisadores inativaram em algumas dessas células dois genes que controlam a expressão de proteínas chamadas antígenos de leucócitos humanos, que direcionam o sistema imunológico às células estranhas. Sem esses marcadores, o sistema imunológico não pode facilmente reconhecer e destruir as células doadoras.
Para evitar ainda mais a detecção do sistema imunológico, a equipe fez algumas células expressarem níveis mais altos de um gene que desencoraja ataques pelas células assassinas e macrófagos naturais do corpo, dois tipos de células imunes. Três meses após o tratamento, embora o sistema imunológico tenha atacado algumas células no enxerto, ele deixou as células que tinham os genes inativados e o gene superexpressado sozinho. Os exames de sangue não mostraram ativação mensurável de células imunológicas ou produção de anticorpos em resposta a essas células.
Antes do transplante, o participante não tinha insulina produzida naturalmente mensurável e estava recebendo doses diárias do hormônio. Mas dentro de quatro a 12 semanas após o transplante, seus níveis aumentaram ligeiramente por conta própria – apresentando que as novas células beta estavam liberando um pouco de insulina em resposta à glicose. Ocorreram quatro eventos adversos, mas nenhum era grave ou relacionado às células modificadas.
O avanço “é incrível”, diz Laura Alonso, chefe da Divisão de Endocrinologia, Diabetes e Metabolismo na Weill Cornell Medicine, que não esteve envolvida no novo estudo. Ao contrário do diabetes tipo 2, no qual as pessoas têm células beta com mau funcionamento, o diabetes tipo 1 pode destruir completamente as células beta. Algumas pessoas com diabetes tipo 1 ainda podem ter um pequeno conjunto de células beta funcionais, mas em casos mais estabelecidos, o sistema imunológico geralmente afasta todas as células, diz Alonso. Para esses casos estabelecidos, ela diz: “A terapia baseada em células é para onde precisamos ir”.
Alonso acrescenta, no entanto, que, embora o novo estudo seja promissor, envolveu apenas um participante e, portanto, é preliminar. E o monitoramento a longo prazo é necessário para confirmar a segurança da terapia antes que possa ser oferecida a mais pessoas. Ela também observa que as células injetadas produziram apenas 7 % da insulina necessária para que uma pessoa seja totalmente independente de medicamentos adicionais. Os pesquisadores forneceram ao destinatário doses de insulina para manter níveis saudáveis de açúcar no sangue.
“É uma descoberta relativamente curta, mas ainda importante”, diz Kevan Herold, endocrinologista da Escola de Medicina de Yale, que também não esteve envolvido no estudo. Como o participante ainda exigia uma quantidade substancial de insulina após o transplante e nenhum outro recebeu esse tratamento, Harold alerta que “o significado clínico não tem um pouco de compra”.
Carlsson diz que a equipe continuará monitorando o destinatário do transplante no próximo ano e aumentará a dose das células modificadas se não ocorrerem efeitos adversos. Enquanto isso, ele e seus colegas estão desenvolvendo uma fonte de células-tronco que seria capaz de produzir grandes quantidades de células produtoras de insulina. “A combinação desses dois avanços criaria a possibilidade de uma cura para o diabetes tipo 1”, diz ele.
Enquanto Herold pensa que ainda é muito cedo para considerar essa abordagem para uma cura, “essas opções estão agora aqui para mudar a doença de maneiras que nunca foram possíveis antes”, diz ele. “Há uma tremenda esperança.”




